Aujourd'hui, c'est #Vulgadredi, comme tous les #VendrediVulga. Et aujourd'hui, on va tellement entrer dans les détails qu'on va même couper des atomes en morceaux. Quand on connaît l'étymologie du mot, c'est un peu bizarre, mais bon, c'est comme ça. En tout cas, pas la peine de s'inquiéter non plus, ça va rester très accessible :-) Et durer seize pouets, comme d'habitude.
La base, vous la connaissez déjà : un atome, c'est un noyau, constitué de protons et de neutrons (qui peuvent d'ailleurs être regroupés sous le nom de « nucléons »), et des électrons qui tournent autour. Contrairement à ce qu'on pourrait croire, ça ne ressemble pas à un mini-système solaire pour autant, mais ça on en reparlera quand on parlera de physique quantique. Pour le moment, concentrons-nous sur le noyau.
La base, vous la connaissez déjà : un atome, c'est un noyau, constitué de protons et de neutrons (qui peuvent d'ailleurs être regroupés sous le nom de « nucléons »), et des électrons qui tournent autour. Contrairement à ce qu'on pourrait croire, ça ne ressemble pas à un mini-système solaire pour autant, mais ça on en reparlera quand on parlera de physique quantique. Pour le moment, concentrons-nous sur le noyau.

2/16 J'ai déjà mentionné la semaine dernière que la taille d'un nucléon est, en nombre d'ordres de grandeurs, un peu plus proche de nous que nous le sommes d'une année-lumière. J'ai également mentionné qu'ils étaient eux-mêmes constitués de particules plus petites, les quarks. Commençons donc par préciser ça un peu. Il existe plusieurs sortes de quarks, mais seulement deux constituent les nucléons.
On appelle ces deux variétés de quarks « up » et « down », et ce qui va les différencier est leur charge électrique. Ces charges sont opposées, et celle du quark « up » est, en valeur absolue, deux fois plus importante que celle du « down ». Ce qui veut dire que, quand on combine deux quarks « down » et un quark « up », on a des charges électriques qui se compensent parfaitement, et le résultat est neutre électriquement : c'est un neutron.
Oh, j'ai eu peu de réactions au thread de la semaine dernière, donc si vous l'avez manqué, il est là : https://fadrienn.irlnc.org/notice/B0TuiSURCfVA9ialuq
On appelle ces deux variétés de quarks « up » et « down », et ce qui va les différencier est leur charge électrique. Ces charges sont opposées, et celle du quark « up » est, en valeur absolue, deux fois plus importante que celle du « down ». Ce qui veut dire que, quand on combine deux quarks « down » et un quark « up », on a des charges électriques qui se compensent parfaitement, et le résultat est neutre électriquement : c'est un neutron.
Oh, j'ai eu peu de réactions au thread de la semaine dernière, donc si vous l'avez manqué, il est là : https://fadrienn.irlnc.org/notice/B0TuiSURCfVA9ialuq
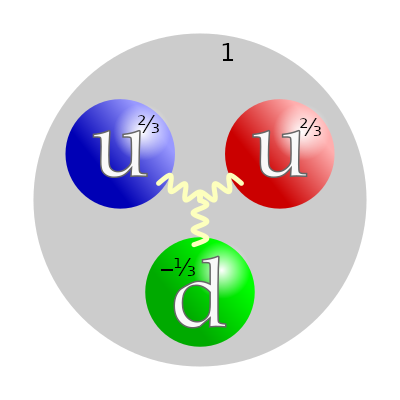
3/16 À l'inverse, quand on combine deux quarks « up » et un quark « down », on obtient une particule chargée électriquement, le proton. Or, il se trouve que la charge d'un électron correspond à trois fois celle d'un quark « down » : un proton a donc une charge de même valeur que celle d'un électron mais qui lui est opposée. Un atome, comportant autant d'électrons autour de lui qu'il ne comporte de protons dans son noyau, est donc globalement électriquement neutre.
Quand il n'y a pas le bon compte d'électrons, ce à quoi on a affaire n'est pas appelé « atome », mais « ion ». Plus précisément, s'il y a plus d'électrons que de protons, on a affaire à un anion, et s'il y en a moins, à un cation. Mais on rentrera peut-être dans les détails à ce sujet une autre fois, pour l'instant, restons en au niveau des noyaux atomiques.
Quand il n'y a pas le bon compte d'électrons, ce à quoi on a affaire n'est pas appelé « atome », mais « ion ». Plus précisément, s'il y a plus d'électrons que de protons, on a affaire à un anion, et s'il y en a moins, à un cation. Mais on rentrera peut-être dans les détails à ce sujet une autre fois, pour l'instant, restons en au niveau des noyaux atomiques.
4/16 Et parlons donc plutôt du nombre de protons qu'il y a dans ces noyaux. C'est un nombre assez important, vous l'aurez compris, car il détermine le nombre d'électrons, et donc le nombre de possibilités d'interactions : échanger des électrons (ou les partager pour former des molécules) est pour beaucoup dans la façon dont les atomes interagissent entre eux, et donc changer un peu le nombre de protons dans le noyau va avoir de grandes conséquences sur le comportement de notre atome.
Or ce nombre dépend de la façon dont l'atome a été formé. J'ai déjà évoqué rapidement ce sujet à plusieurs reprises dans les précédent threads, il est peut-être temps de détailler un peu plus (En fait, j'ai déjà lié ici deux articles de blogs où je parlais de ça, mais autant en redire quelques bouts directement). À la base, donc, tout commence avec ce « Big Bang » que j'évoquais récemment.
Pour un peu de contexte général sur ce truc et comment on l'a découvert et nommé, voyez donc le thread d'il y a deux semaines : https://fadrienn.irlnc.org/notice/B0FBBndEMU321GJpGC
Or ce nombre dépend de la façon dont l'atome a été formé. J'ai déjà évoqué rapidement ce sujet à plusieurs reprises dans les précédent threads, il est peut-être temps de détailler un peu plus (En fait, j'ai déjà lié ici deux articles de blogs où je parlais de ça, mais autant en redire quelques bouts directement). À la base, donc, tout commence avec ce « Big Bang » que j'évoquais récemment.
Pour un peu de contexte général sur ce truc et comment on l'a découvert et nommé, voyez donc le thread d'il y a deux semaines : https://fadrienn.irlnc.org/notice/B0FBBndEMU321GJpGC
5/16 Dans les premières secondes de notre univers, ou plutôt dans les premières secondes après ce que l'on appelle le « mur de Planck » (promis, j'arrête de teaser et je donne des détails sur tous ces trucs nommés d'après Max Planck dans un prochain thread), les quarks, qui ne se baladent isolés que dans des conditions particulièrement extrêmes, se sont assemblés entre eux pour former des nucléons.
Ces nucléons commencent à s'assembler entre eux pour former des noyaux d'atomes dans les vingt minutes qui suivent, mais cela ne forme qu'une petite proportion de noyaux, dont les plus lourds ne comptent tout au plus qu'une dizaine de nucléons (dont jusqu'à cinq protons). Ce qui est assez peu par rapport aux éléments les plus lourds que nous connaissons.
Si vous voulez une version avec un peu plus de détails et le rôle d'autres particules, voyez là, donc : https://fadrienn.irlnc.org/articles/sciences/poussieres_detoiles/ et https://fadrienn.irlnc.org/articles/sciences/poussieres_detoiles2/
Ces nucléons commencent à s'assembler entre eux pour former des noyaux d'atomes dans les vingt minutes qui suivent, mais cela ne forme qu'une petite proportion de noyaux, dont les plus lourds ne comptent tout au plus qu'une dizaine de nucléons (dont jusqu'à cinq protons). Ce qui est assez peu par rapport aux éléments les plus lourds que nous connaissons.
Si vous voulez une version avec un peu plus de détails et le rôle d'autres particules, voyez là, donc : https://fadrienn.irlnc.org/articles/sciences/poussieres_detoiles/ et https://fadrienn.irlnc.org/articles/sciences/poussieres_detoiles2/
6/16 Il faut dire que vingt minutes, c'est assez court. Mais passé cette durée, l'expansion de l'univers a joué son rôle : les rencontres entre nucléons deviennent moins fréquentes, alors que la quantité de rayonnement ambiant est encore assez importante pour séparer les groupes ainsi formés. Le bilan net des premiers instants de l'univers nous laisse donc en grande majorité des protons isolés les uns des autres.
Mais un proton isolé est après tout à lui seul un noyau d'atome tout à fait convenable : lorsque les choses se calment autour de lui et qu'il finit par se doter d'un électron, cela donne quelque chose auquel nous avons donné le nom d'« hydrogène », qui est un élément important de pas mal de molécules et de réactions chimiques, notamment celles qui constituent le vivant.
Mais un proton isolé est après tout à lui seul un noyau d'atome tout à fait convenable : lorsque les choses se calment autour de lui et qu'il finit par se doter d'un électron, cela donne quelque chose auquel nous avons donné le nom d'« hydrogène », qui est un élément important de pas mal de molécules et de réactions chimiques, notamment celles qui constituent le vivant.
7/16 L'hydrogène est donc l'élément le plus abondant de l'univers, et l'écrasante majorité de celui que nous rencontrons autour de nous date directement du Big Bang. Le reste de ce qui nous constitue, en revanche, a donc essentiellement dû être fabriqué plus tard. Ce sont en fait les étoiles qui s'en sont chargé, car, en leur cœur, les conditions de température et de pression sont telles que les électrons sont séparés des protons et que l'endroit commence à ressembler à l'univers des vingt premières minutes… mais cette fois-ci sans expansion et donc pour plusieurs centaines de millions d'années au moins.
Pendant la première phase de la vie des étoiles, la fusion nucléaire qui règne dans leur cœur produit des noyaux constitués de quatre nucléons : deux protons et deux neutrons. Nous appelons ça un noyau d'hélium. Quand l'hydrogène commence à manquer (dans le cœur, en tout cas, ça reste son constituant principal si on prend toute l'étoile en compte), les changements de dynamique interne la font gonfler et devenir une géante rouge.
J'avais déjà mentionné ce point dans mon thread sur les nébuleuses et la vie et la mort des étoiles, je vous le remet : https://fadrienn.irlnc.org/notice/AxffZGekWdb41yY0OW
Pendant la première phase de la vie des étoiles, la fusion nucléaire qui règne dans leur cœur produit des noyaux constitués de quatre nucléons : deux protons et deux neutrons. Nous appelons ça un noyau d'hélium. Quand l'hydrogène commence à manquer (dans le cœur, en tout cas, ça reste son constituant principal si on prend toute l'étoile en compte), les changements de dynamique interne la font gonfler et devenir une géante rouge.
J'avais déjà mentionné ce point dans mon thread sur les nébuleuses et la vie et la mort des étoiles, je vous le remet : https://fadrienn.irlnc.org/notice/AxffZGekWdb41yY0OW
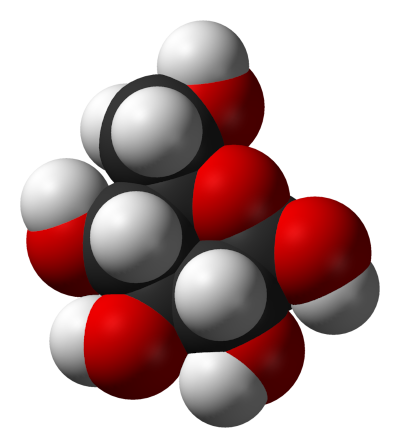
8/16 Au cœur de ces géantes rouges, une autre fusion s'amorce : trois noyaux d'hélium peuvent se rejoindre pour former un noyau contenant six protons (pour généralement douze nucléons, mais on va y revenir). On appelle ça du carbone, et c'est aussi un élément particulièrement important dans les molécules et réactions chimiques du vivant. Si l'étoile est suffisamment massive, d'autres phases de fusion vont s'enchaîner, produisant d'autres éléments, comme l'oxygène, comportant huit protons.
Toutefois, même les conditions extrêmes régnant au cœur des étoiles les plus massives ne sont pas suffisantes pour former les éléments les plus lourds. Car l'oxygène, avec ses huit protons, reste très léger, comparé à l'uranium qui en compte 92, et qui ne peut pas vraiment se former là. Une (bonne) partie de nos atomes provient donc des étoiles, mais d'autres phénomènes doivent également intervenir.
Pour (un peu) plus de détails sur ce qui se passe quand une étoile est assez lourde pour former des éléments plus lourds, voyez mon thread sur ce qu'elles deviennent ensuite : https://fadrienn.irlnc.org/notice/AxtkWaoCMXHreCwxYe
Toutefois, même les conditions extrêmes régnant au cœur des étoiles les plus massives ne sont pas suffisantes pour former les éléments les plus lourds. Car l'oxygène, avec ses huit protons, reste très léger, comparé à l'uranium qui en compte 92, et qui ne peut pas vraiment se former là. Une (bonne) partie de nos atomes provient donc des étoiles, mais d'autres phénomènes doivent également intervenir.
Pour (un peu) plus de détails sur ce qui se passe quand une étoile est assez lourde pour former des éléments plus lourds, voyez mon thread sur ce qu'elles deviennent ensuite : https://fadrienn.irlnc.org/notice/AxtkWaoCMXHreCwxYe
9/16 Quelles conditions encore pire que celles qu'on rencontre au cœur des étoiles les plus massives peuvent former des éléments aussi lourds ? Celles que l'on rencontre lors de la fusion de deux étoiles à neutrons. Ces événements, sans doute les plus impressionnants de l'univers, sont les seuls qui parviennent à produire des éléments lourds comme l'uranium, mais aussi l'argent (47 protons), le platine (78) et l'or (79).
Si ces éléments sont beaucoup moins utiles à la chimie du vivant, on les retrouve donc cependant, selon le cas, dans nos centrales nucléaires ou dans nos bijouteries. Il y a ce lieu commun selon lequel nous sommes poussières d'étoiles, mais tous les aspects de l'univers ont pu avoir leur influence sur nous d'une façon ou d'une autre.
Vous voudriez savoir quel phénomène est majoritairement à l'origine de chaque élément ? J'ai vu passer ici une super image à ce sujet, donc n'hésitez pas à aller liker/booster ça : https://mastodon.social/@coreyspowell/113907625463172223
Si ces éléments sont beaucoup moins utiles à la chimie du vivant, on les retrouve donc cependant, selon le cas, dans nos centrales nucléaires ou dans nos bijouteries. Il y a ce lieu commun selon lequel nous sommes poussières d'étoiles, mais tous les aspects de l'univers ont pu avoir leur influence sur nous d'une façon ou d'une autre.
Vous voudriez savoir quel phénomène est majoritairement à l'origine de chaque élément ? J'ai vu passer ici une super image à ce sujet, donc n'hésitez pas à aller liker/booster ça : https://mastodon.social/@coreyspowell/113907625463172223
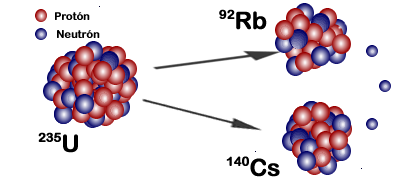
10/16 Vous aurez d'ailleurs peut-être remarqué sur cette image la présence d'éléments dont l'origine principale est la désintégration nucléaire. Ou vous aurez peut-être pensé à ce phénomène dès que j'ai mentionné l'uranium. De quoi s'agit-il exactement ? Il se trouve que certains noyaux sont instables et peuvent donc se désintégrer, éjectant quelques uns de leurs nucléons voire carrément se cassant en morceaux.
Ça concerne facilement les noyaux les plus lourds. En effet, étant tous chargés de façon équivalente, les protons se repoussent les uns les autres, et un noyau comme celui de l'uranium, par exemple, ne peut pas rester stable éternellement. Mais cela concerne également des noyaux plus léger… en tout cas dans certaines de leurs configurations.
Ça concerne facilement les noyaux les plus lourds. En effet, étant tous chargés de façon équivalente, les protons se repoussent les uns les autres, et un noyau comme celui de l'uranium, par exemple, ne peut pas rester stable éternellement. Mais cela concerne également des noyaux plus léger… en tout cas dans certaines de leurs configurations.
11/16 En effet, si le nombre de protons est caractéristique du type d'atome dont il est question, le nombre de neutrons, lui, peut parfois varier. Ainsi, le carbone a toujours six protons, sinon ce ne serait plus du carbone ; mais il peut parfaitement avoir six, sept ou huit neutrons. Ces différentes variations sont appelées des « isotopes ».
Si vous faites la somme de tous les nucléons, le carbone à six neutrons possède donc douze particules dans son noyau. On l'appelle donc cet isotope en particulier « carbone-12 ». C'est celui qu'on croise le plus souvent, et qui est parfaitement stable. L'isotope de carbone possédant huit neutrons est appelé pour sa part, et de la même façon, « carbone-14 », et celui-ci est loin d'être aussi stable, et finit donc par se désintégrer.
Si vous faites la somme de tous les nucléons, le carbone à six neutrons possède donc douze particules dans son noyau. On l'appelle donc cet isotope en particulier « carbone-12 ». C'est celui qu'on croise le plus souvent, et qui est parfaitement stable. L'isotope de carbone possédant huit neutrons est appelé pour sa part, et de la même façon, « carbone-14 », et celui-ci est loin d'être aussi stable, et finit donc par se désintégrer.
12/16 Il est impossible de savoir à quel moment un atome donné va se désintégrer. Mais chaque isotope instable possède une « demi-vie » spécifique, une durée de temps au bout de laquelle environ la moitié de l'échantillon considéré (comptant un grand nombre d'atomes) se sera désintégrée. Ce qui peut donc être utilisé pour dater le temps qui passe (avec une légère imprécision).
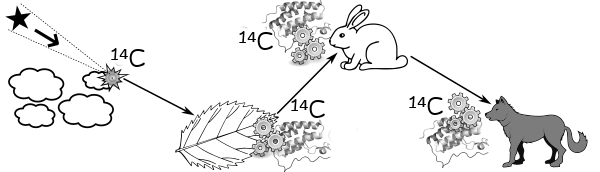
Ainsi, nous autres êtres vivants échangeons du carbone en permanence avec notre environnement, et avons donc une quantité de carbone-14 stable, toujours renouvelée. À notre mort, ces échanges cessent, et la quantité de carbone-14 que nous contenons ne fait donc plus que diminuer. En mesurant combien il reste de carbone-14 dans une matière issue d'un être vivant, comme du bois, on peut donc dater approximativement de quelle époque il date.
Ainsi, nous autres êtres vivants échangeons du carbone en permanence avec notre environnement, et avons donc une quantité de carbone-14 stable, toujours renouvelée. À notre mort, ces échanges cessent, et la quantité de carbone-14 que nous contenons ne fait donc plus que diminuer. En mesurant combien il reste de carbone-14 dans une matière issue d'un être vivant, comme du bois, on peut donc dater approximativement de quelle époque il date.

13/16 Les neutrons, même s'ils n'ont pas de charge électrique, possèdent néanmoins une masse. Même lorsqu'ils forment une configuration stable et ne conduisent pas les noyaux atomiques à se désintégrer, les différents isotopes ont donc une certaine influence sur certaines propriétés de l'atome. Évidemment, moins le noyau compte de nucléons, plus cette différence a d'impact.
Ainsi, nous avons parlé tout à l'heure de l'atome d'hydrogène dit « hydrogène-1 », qui ne compte qu'un proton. Mais il existe aussi deux autres isotopes : l'« hydrogène-2 », aussi appelé « deutérium », comptant un proton et un neutron, et l'« hydrogène-3 », aussi appelé « tritium », comptant un proton et deux neutrons, avec une masse qui varie donc du simple au triple, ce qui peut avoir une certaine influence.
Ainsi, la molécule d'eau contient deux atomes d'hydrogène. Si ceux-ci sont fait d'un isotope à neutrons, cela donne de l'eau lourde : https://fr.wikipedia.org/wiki/Eau_lourde
Ainsi, nous avons parlé tout à l'heure de l'atome d'hydrogène dit « hydrogène-1 », qui ne compte qu'un proton. Mais il existe aussi deux autres isotopes : l'« hydrogène-2 », aussi appelé « deutérium », comptant un proton et un neutron, et l'« hydrogène-3 », aussi appelé « tritium », comptant un proton et deux neutrons, avec une masse qui varie donc du simple au triple, ce qui peut avoir une certaine influence.
Ainsi, la molécule d'eau contient deux atomes d'hydrogène. Si ceux-ci sont fait d'un isotope à neutrons, cela donne de l'eau lourde : https://fr.wikipedia.org/wiki/Eau_lourde
14/16 Mais les propriétés liées à la charge électrique, et donc au nombre de protons, pour leur part, sont communes à tous les isotopes d'un même élément chimique. Certaines sont d'ailleurs plus ou moins similaires chez plusieurs éléments chimiques, formant donc des familles. Ainsi, les « gaz rares » sont caractérisés par le fait que leur disposition d'électrons fait qu'ils interagissent peu avec les autres molécules.
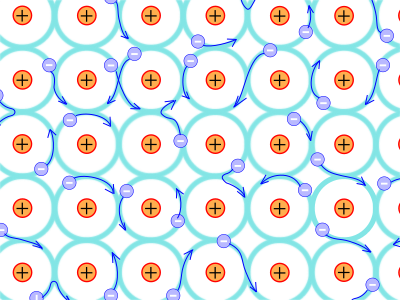
Plus communs, les métaux sont caractérisés par le fait que les électrons passent facilement d'un atome à l'autre (en tout cas dans un matériau constitué essentiellement de métaux, c'est évidemment différent s'il y a plein d'éléments différents), ce qui en fait de bons conducteurs d'électricité, mais également de chaleur. Une grande partie des éléments chimiques connus sont des métaux, ou peuvent se comporter comme des métaux dans certaines conditions.
Plus communs, les métaux sont caractérisés par le fait que les électrons passent facilement d'un atome à l'autre (en tout cas dans un matériau constitué essentiellement de métaux, c'est évidemment différent s'il y a plein d'éléments différents), ce qui en fait de bons conducteurs d'électricité, mais également de chaleur. Une grande partie des éléments chimiques connus sont des métaux, ou peuvent se comporter comme des métaux dans certaines conditions.
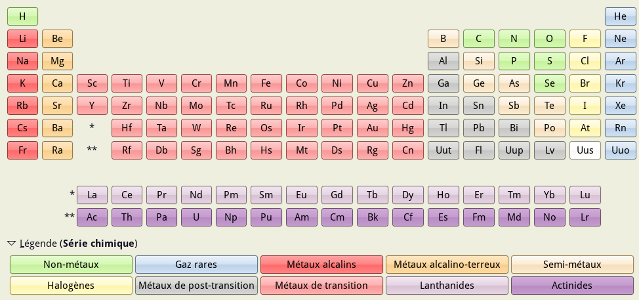
15/16 Pour représenter ces différentes familles, les chimistes regroupent donc ces atomes au sein d'un tableau, appelé le « tableau périodique des éléments ». Les différents éléments y sont rangés selon leur nombre de protons, et les position en ligne, colonne ou diagonal indiquent les propriétés communes.
L'image sus-mentionnée montrant les origines des différents éléments reprenait d'ailleurs la forme de ce tableau, mais il est possible de l'utiliser pour mettre en avant d'autres propriétés. Ce tableau est complet depuis 2002, année où a été synthétisé pour la première fois l'oganesson, comptant 118 protons, hautement instable. Quelques propriétés d'hypothétiques éléments plus lourds ont pu être estimées, mais ceux-ci n'ont jamais pu être produits jusque là. Nous connaissons donc au moins tous les éléments chimiques que l'on peut rencontrer dans l'univers connu.
L'image sus-mentionnée montrant les origines des différents éléments reprenait d'ailleurs la forme de ce tableau, mais il est possible de l'utiliser pour mettre en avant d'autres propriétés. Ce tableau est complet depuis 2002, année où a été synthétisé pour la première fois l'oganesson, comptant 118 protons, hautement instable. Quelques propriétés d'hypothétiques éléments plus lourds ont pu être estimées, mais ceux-ci n'ont jamais pu être produits jusque là. Nous connaissons donc au moins tous les éléments chimiques que l'on peut rencontrer dans l'univers connu.
16/16 Ce tableau est parfois appelé « Tableau de Mendeleïev », du nom de Dmitri Mendeleïev, chimiste russe ayant commencé à élaborer un tableau de ce style en 1869. Nos connaissances, à l'époque, étaient beaucoup moins avancées, cependant : le tableau de Mendeleïev comptait encore pas mal de trous, et le classement à l'époque était fait selon la masse plutôt que selon le nombre de protons, ce qui fait que quelques éléments ont dû être déplacés, même si certaines des idées de base étaient déjà là.
Il est donc préférable de ne plus utiliser ce nom, qui ne correspond plus exactement à ce que l'on utilise aujourd'hui. Mais c'est au moins un bon rappel du fait que la science est quelque chose qui évolue avec le temps, et que, même si j'aborde dans ces threads des choses plutôt bien établies, il n'est pas impossible que certaines soient remises en cause à l'avenir. En attendant, j'espère que ça vous plaît toujours, et à moins d'une chouette suggestion, on parlera probablement plus en détail de physique quantique la semaine prochaine.
Au fait, si vous aimez les formats plus classiques, j'avais mis une partie des éléments de ce thread en article de blog (incluant une version audio) par là : https://fadrienn.irlnc.org/articles/sciences/atomes/
Il est donc préférable de ne plus utiliser ce nom, qui ne correspond plus exactement à ce que l'on utilise aujourd'hui. Mais c'est au moins un bon rappel du fait que la science est quelque chose qui évolue avec le temps, et que, même si j'aborde dans ces threads des choses plutôt bien établies, il n'est pas impossible que certaines soient remises en cause à l'avenir. En attendant, j'espère que ça vous plaît toujours, et à moins d'une chouette suggestion, on parlera probablement plus en détail de physique quantique la semaine prochaine.
Au fait, si vous aimez les formats plus classiques, j'avais mis une partie des éléments de ce thread en article de blog (incluant une version audio) par là : https://fadrienn.irlnc.org/articles/sciences/atomes/
- replies
- 0
- announces
- 0
- likes
- 2