§ Posté le 08/07/2017 à 22h 36m 53
Dans les histoires de fiction, il arrive qu'un engin extra-terrestre soit découvert sur terre (par exemple, une sorte de couffin venu d'une planète sur le point d'exploser(1)). Et il arrive, dans ces cas-là, qu'un personnage l'ayant analysé croit bon de signaler, pour souligner l'exotisme de la chose, que l'objet contient des éléments qui « ne sont pas dans le tableau de Mendeleïev », ou autre formule approchante. Le souci, c'est que, pour peu que vous sachiez un minimum ce dont ce personnage est en train de parler, vous vous rendez compte aussitôt que la personne qui a écrit les dialogues, elle, n'en avait aucune idée…
Enfin, comme à peu près chaque fois qu'il est question de sciences, ça dépend de quand date l'œuvre en question. À l'époque où Dmitri Mendeleïev travaillait sur le tableau en question, soit dans la seconde moitié du dix-neuvième siècle, la remarque se tenait, mais les œuvres de fiction y faisant référence étaient moins nombreuses.
À l'origine de ce tableau, en effet, se trouve la notion d'élément chimique. Ces éléments chimiques sont les éléments de base qui composent la matière qui nous entoure. Les noms de certains de ces éléments ont d'ailleurs toutes les chances de vous être familiers : oxygène, azote, carbone, fer, cuivre, hydrogène… Pour comprendre ce que sont exactement ces éléments, il est nécessaire de se pencher sur une notion que j'avais déjà évoquée : celle d'atomes.
Ce nom, signifiant « insécable », vient à l'origine d'un courant philosophique de la Grèce antique, que nous connaissons principalement par les œuvres de Démocrite : l'atomisme. Les atomes scientifiques ont été nommés ainsi parce qu'au moment de leur découverte, ils semblaient correspondre à la définition philosophique du terme. Mais, les choses n'étant jamais figées en sciences, on a fini par découvrir que ces « atomes » n'étaient pas vraiment insécables, mais pouvaient eux-mêmes être subdivisés. On leur a tout de même gardé ce nom.
Allons donc voir « dans » ces atomes de quoi ils sont faits 
D'abord, les couches externes : elle sont composées d'électrons, c'est-à-dire de petites particules de matière qui présentent une charge électrique. Ces électrons se déplacent(2) autour de la couche centrale de l'atome, appelée « noyau », qui est pour sa part constituée de deux autres sortes de particules : les neutrons, électriquement neutres, et les protons, qui présentent une charge aussi forte que celle des électrons, mais qui lui est opposée. Puisque ces particules forment le noyau des atomes, on les regroupe toutes deux sous le terme de « nucléons ».
Conventionnellement, on considère la charge du proton comme étant l'unité de base pour mesurer les charges électriques : un proton a donc une charge de 1e, et l'électron, qui lui est opposé, a donc une charge de -1e. Le neutron, étant neutre, a pour sa part une charge de 0(3), et un atome normalement constitué ayant autant de protons que d'électrons, il est donc, globalement, électriquement neutre.
Il arrive toutefois qu'un atome perde un ou plusieurs de ses électrons, ou au contraire gagne quelques électrons « de trop ». Il devient dans ce cas ce que l'on appelle un « ion », chargé électriquement. On parle, plus précisément, de « cation » quand cette charge est positive (donc qu'il « manque » des électrons par rapport à l'atome correspondant), et d'« anion » quand elle est négative (donc qu'il y a des électrons « en trop »).
Toutefois, toutes les combinaisons d'ions ne sont pas possibles en pratique. Les attractions et répulsions électriques entre les particules (un proton et un électron s'attirent ; deux protons se repoussent, comme le font deux électrons) font que les électrons sont disposés en « couches » autour du noyau, et seule la plus externe de ces couches peut perdre ou gagner des électrons, en nombre limité. Le nombre de protons dans le noyau détermine donc la disposition des électrons « en couches »(4), et par là les possibilités qu'il y aura de former tel ou tel ion.
Là où la chose est particulièrement importante, c'est que c'est également ce qui détermine la façon dont les différents atomes vont pouvoir s'assembler entre eux pour former des molécules. Ainsi, une molécule d'eau est constituée de deux atomes d'hydrogène et d'un atome d'oxygène (« H20 »), ce qui est possible parce que les couches externes des trois atomes qui la constituent sont compatibles. Si on remplace l'atome d'oxygène par un atome de carbone, il ne faut plus deux, mais quatre atomes d'hydrogène (« CH4 », méthane) pour réussir à obtenir une molécule stable.
Or, c'est de la façon dont les atomes – qui la constituent – se combinent entre eux que viennent les propriétés de la matière qui nous entoure. Le nombre de protons que contient un noyau d'atome est donc le critère fondamental qui détermine ce qu'est cet atome et ce qu'il va pouvoir faire avec ses voisins. Si l'atome possède un seul proton, c'est un Hydrogène. S'il en possède deux, c'est un Hélium. S'il en possède trois, un Lithium. S'il en possède quatre, un Béryllium. Pour cinq, un Bore. Pour six, un Carbone. Pour sept, un Azote. Pour huit, un Oxygène. Je ne continue pas plus loin ici : la liste est assez longue.
Or, classer les éléments en fonction de leur nombre de protons (ou « numéro atomique ») est la première fonction du tableau dont il était question. Dmitri Mendeleïev lui-même, à l'époque, le représentait avec des trous, parce que certains atomes n'avaient pas encore été identifiés. Mais les chercheurs ont pas mal travaillé, depuis cette époque, à boucher ces trous.
Le tableau périodique des éléments, dans sa version actuellement utilisée, est donc complet : il ne reste plus de place à un mystérieux élément extraterrestre pour venir s'y glisser(5).
La seule possibilité de trouver un élément chimique qui ne s'intègre pas (encore) au tableau, ce serait qu'il ait davantage(6) de protons que l'élément qui est actuellement en dernière position (à l'instant où j'écris ces lignes, si ça vous intéresse, il semble que ce dernier soit l'oganesson, comptant 118 protons. Quand je vous disais que la liste était longue).
Or, il y a un léger obstacle au fait qu'un tel élément puisse se retrouver dans un vaisseau extraterrestre : le fait qu'il serait totalement instable.
En effet, comme nous l'avons vu, deux protons portent une charge électrique de même signe, et donc se repoussent mutuellement. Au sein d'un noyau d'atomes, les différents nucléons sont fortement reliés entre eux, mais, si l'on met trop de protons, il vient toujours un moment où la répulsion devient trop forte et où tout ou partie des protons finira par se séparer du reste, disloquant ainsi l'atome. À partir de l'uranium, comptant 92 protons, aucun élément n'est suffisamment stable pour ne pas finir par se désagréger (en plus ou moins longtemps, mais nous aborderons les questions de radioactivité une autre fois).
Et quand bien même, quoique nous n'ayons jamais pu observer ces éléments « superlourds », beaucoup trop instables, leur classement est théoriquement prévu.
Quoique le seul nombre de protons détermine pas mal des propriétés de l'atome, il ne faudrait pour autant pas croire qu'il n'y a que lui qui compte. Comme nous l'avons vu, les noyaux d'atomes contiennent également des neutrons qui, quoiqu'électriquement neutres, ont tout de même quelque chose d'assez important : une masse.
Pour un nombre de protons donné, les atomes sont donc plus ou moins lourds en fonction du nombre de neutrons qu'ils contiennent. Le nombre total de nucléons est donc la deuxième grande caractéristique qui sert à identifier les noyaux d'atomes.
Dans la plupart des cas, un atome d'un type donné va avoir le même nombre de nucléons que ses semblables. Par exemple, les noyaux de carbone sont généralement constitués de six protons et de six neutrons, soit douze nucléons. Cependant, il existe également, en beaucoup plus petite quantité, des noyaux de carbones contenant huit neutrons en plus de leurs six protons : dotés de quatorze nucléons, ils forment le fameux « carbone 14 » servant pour les datations (j'en reparlerai en abordant la radioactivité). La même chose vaut pour les autres atomes, qui ont donc plusieurs formes possibles (on parle d'« isotope »).
Un autre exemple assez connu est celui de l'hydrogène. Son isotope (sa forme) le plus courant se présente comme un seul proton, sans neutron à côté. C'est donc de l'« hydrogène 1 ». Mais il existe également deux autres isotopes (deux autres formes) : l'« hydrogène 2 » (ou deutérium), constitué d'un proton et d'un neutron, donc de deux nucléons, et l'« hydrogène 3 » (ou tritium), constitué d'un proton et de deux neutrons, donc de trois nucléons.
Ayant toujours un seul proton, les trois isotopes d'hydrogène peuvent s'associer de la même manière aux autres atomes pour former des molécules. Pour autant, la différence de masse est si grande, proportionnellement parlant (le deutérium est deux fois plus lourd que l'hydrogène 1) que les molécules ainsi formées peuvent avoir des propriétés assez différentes. On peut citer, principalement, l'eau lourde.
La chose est assez importante, sur le plan historique, car à l'époque où l'on a commencé à vouloir classer les éléments chimiques, c'est la masse atomique de l'isotope le plus fréquent que l'on utilisait, et non pas le nombre de protons. Or, la répartition des neutrons fait que certains atomes sont plus légers que d'autres en ayant davantage de protons.
Ainsi, l'isotope le plus courant du tellure (qui compte 52 protons) contient 130 nucléons au total. L'iode, doté pour sa part de 53 protons, se présente le plus souvent avec 127 nucléons : selon le critère choisi, il y a donc besoin d'inverser leurs places dans le tableau.
C'est plus qu'un simple petit détail, car le tableau range également les éléments en fonction de leurs familles : l'iode est un halogène, comme les trois éléments qui le précèdent en colonne, tandis que le tellure est un métalloïde, comme les trois éléments qui le précèdent en diagonal.
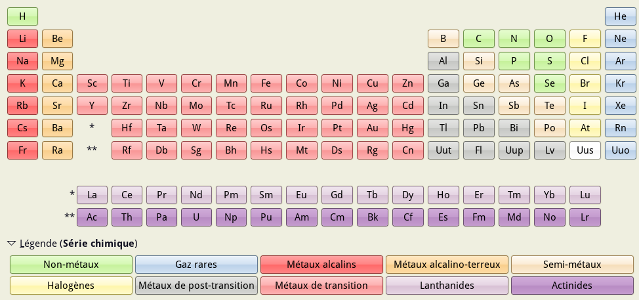
(Cette capture provient du logiciel gelemental, contenant pas mal d'infos sur les éléments)
C'est la raison pour laquelle l'appellation « tableau de Mendeleïev » devrait être évitée aujourd'hui : le tableau périodique que nous utilisons désormais ne correspond plus à celui que proposait autrefois le chimiste russe. Le changement de critère d'ordonnancement a permis de résoudre les quelques problèmes de classification qui le laissaient perplexe à l'époque.
La grande force de ce tableau, dans son état actuel, est de permettre de visualiser facilement les différentes familles d'éléments, et donc de leurs propriétés physiques et chimiques. Pour l'ensemble des éléments qui constituent l'univers observable(7).
Ce que certaines personnes écrivant de la fiction semblent ne pas avoir compris, c'est que l'univers n'est pas un « multivers » : les planètes distantes sont composées des mêmes éléments que la nôtre(7) (même si les quantités peuvent varier. Ainsi, l'iridium semble davantage présent dans certaines météorites qu'à la surface de notre planète).
Bien sûr, ça ne doit pas empêcher, pour les besoins de l'histoire, d'inventer un matériau imaginaire, mais dans ce cas, autant éviter de mettre précisément l'accent sur une incohérence. Par exemple, le mithril et le vibranium sont présentés comme des métaux jusque là inconnus, ce qui est impossible (le groupe des métaux est une partie, complète elle aussi, du tableau périodique). Mais comme on ne vous colle pas la raison pour laquelle c'est impossible sous le nez en vous en parlant, ça facilite un peu la suspension consentie d'incrédulité.
Après, on peut faire encore mieux, en présentant la chose comme un minerai (c'est le cas pour le naqahdah, par exemple) : ceux-ci sont en effet des composés complexes, et non pas des éléments simples, ce qui laisse largement plus de marge de manœuvre. Il arrive même que ça puisse donner des surprises intéressantes.
Dans tout les cas, il reste surtout à ne pas oublier qu'irréaliste ne veut pas dire incohérent.